受試者申訴/建言/諮詢
IRB專線:03-8241268
受試者保護中心專線:03-8241231
E-mail:irb@mch.org.tw
受試者保護中心架構
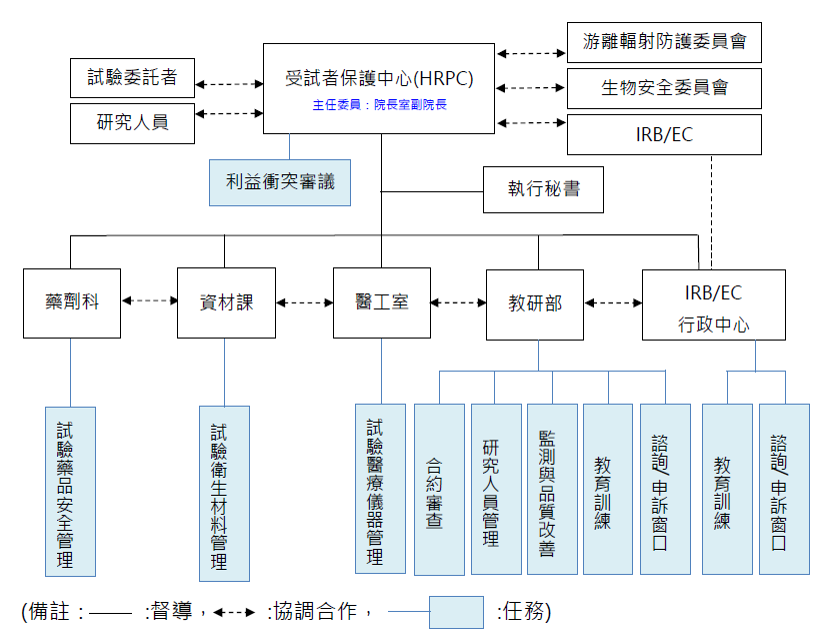
受試者保護任務
本院設有受試者保護中心,負責以下受試者(研究對象)保護任務:
1.本院受試者保護方針與策略之規劃。
2.受試者保護業務之統合、協調、管理與監督 。
3.受試者保護業務之稽核與品質改善 。
4.負責審查與管理「研究機構」之利益衝突,針對具有利益衝突的案件,提供減免、迴避利益衝突之處置建議 。
5.受理人體研究之受試者、研究人員以及其他人士,對本院臨床研究受試者保護相關業務之諮詢、申訴或建議 。
6.配合辦理人體研究倫理審查委員會暨受試者保護查核作業 。
7.臨床試驗合約審查之安排與監督。
利益衝突與迴避管理
1. 我們針對顯著財務利益及非財務關係進行揭露、必要時之審查相對應管理。負責單位為本院人體試驗暨研究倫理委員會。
2. 研究團隊成員需申報範圍包含個人、及其配偶、未成年子女,從試驗/研究計畫委託者收受之報酬、捐贈、禮品、
其他具金錢價值之給付,或對其資產持股利益達資本額5%或價值超過新台幣150,000元之顯著財務利益。
3. 每件IRB新案、期中/追蹤報告送審時,均需填具研究人員財務利益衝突申報表 。於變更時亦需揭露,以利利益衝突管理。
4. 各項申報須知及定義,依本院人體試驗暨研究倫理委員會-保密和利益衝突與迴避管理標準書及相關申報表單辦理。
公告事項
- 衛生福利部食品藥物管理署網站公告之「藥品臨床試驗受試者保護手冊」(2024/12/03來函)
更新日期:2024年12月11日
網頁維護者:朱珮儀課長
更新日期:2025/01/07 公告單位:教研部